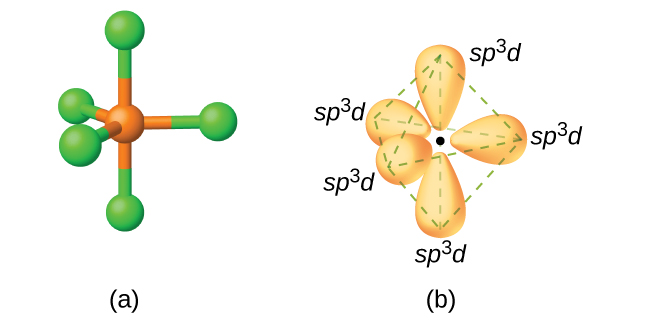
为什么 spd 杂化形成的是键角不等的三角双锥?

对电子 a 正四面体 只有一种角度,109&
> 题目详情

4个电子,o不供给电子,s的价电子数6,6 4=10,应该是5对电子对,成键5对

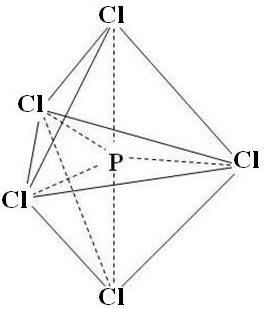
dsp3d3sp三角双锥配合物离子的空间构型
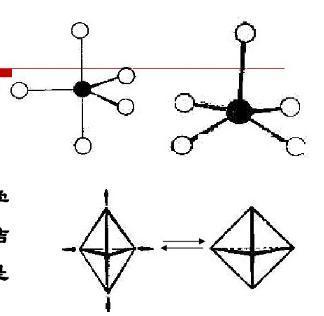
三角双锥

第2章 配合物的结构和成键理论ppt 配位数 5 5 6 几何构型 三角双锥
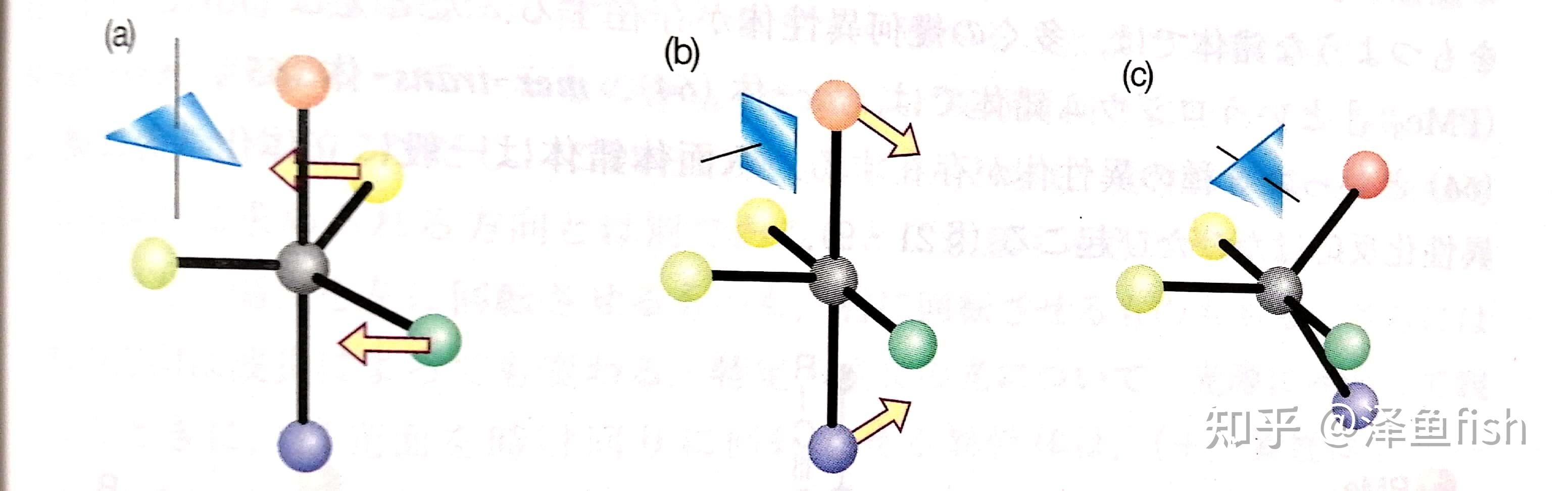
五配位:三角双锥形和四方锥形配合物
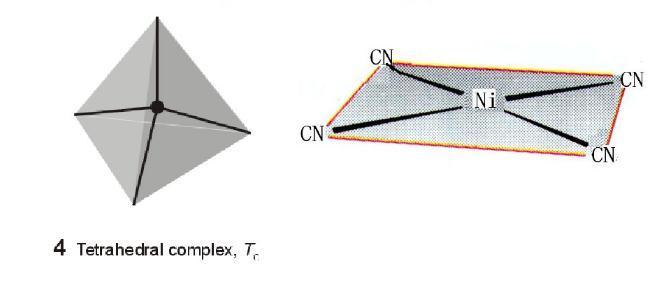
三角双锥

六原子分子……三角双锥型

vp 2 3 4 5 6 模型 直线形 平面三角形 正四面体 三角双锥体 正八面体
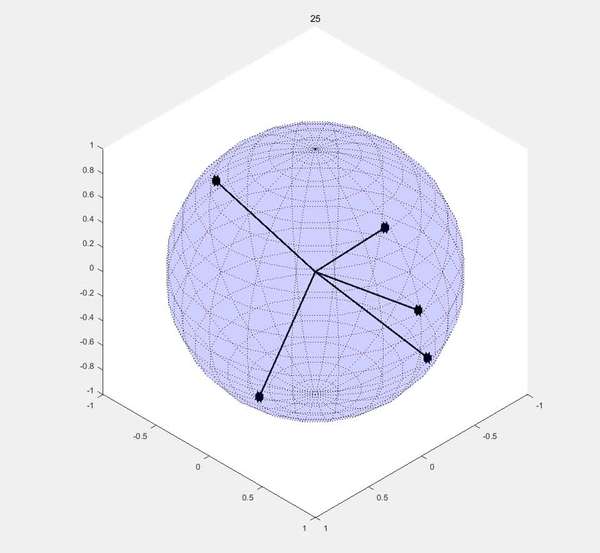
为什么 spd 杂化形成的是键角不等的三角双锥?

6)what三角双锥trigonal bipyramidal三角双锥形trigonal pyramidal

4 5 正四面体 三角双锥 正八面体 五角双锥 确定电子对的空间

基于上面的结论,他们发现在由三角双锥体配位通过共享顶角而构成的

孤对电子占据的位置: vp = 5,电子对空间构型为三角双锥, lp占据轴向

ch so32 m n数 数 价电子空间分布 四面体 三角双锥

结构: 由于硼是缺电子结构,三氟化硼形成一个4中心6电子的大π键

下列化合物分子中一定既含单键又含双键的是( )
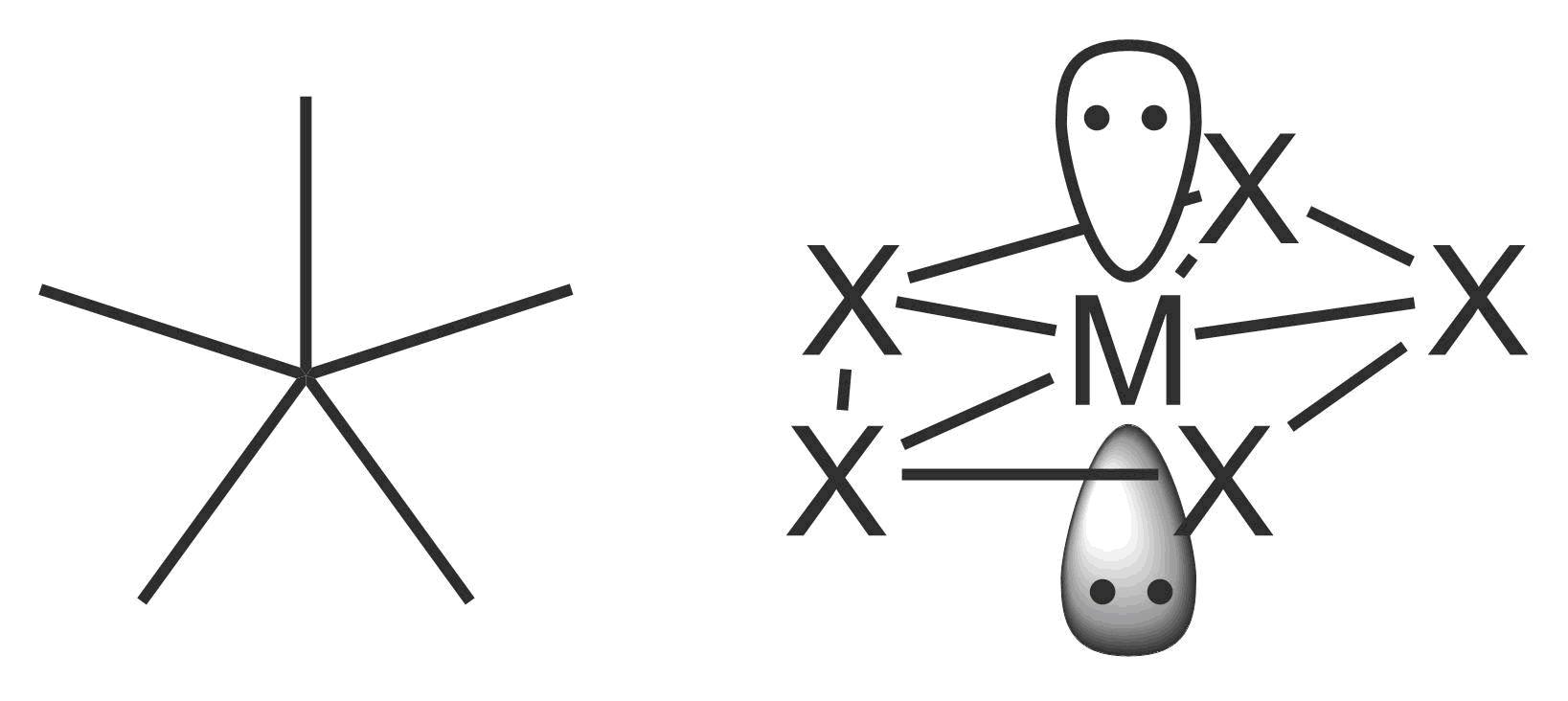
为什么sp06d杂化形成的是键角不等的三角双锥

空间构型 分子的 空间构型 例 sf4 clf3 xef2 1 2 三角双锥 三角双

三角双锥

无机分子的立体结构

展开全部 三角双锥 向左转 向右转
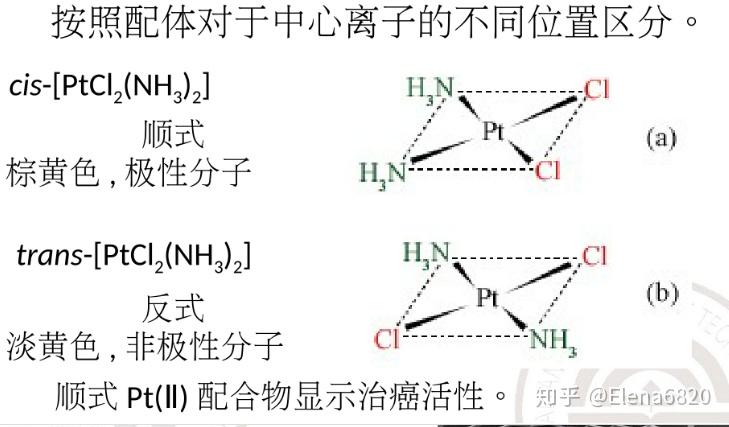
配合物的异构现象(结构决定性质3feco三角双锥:配位数为5;例:;61
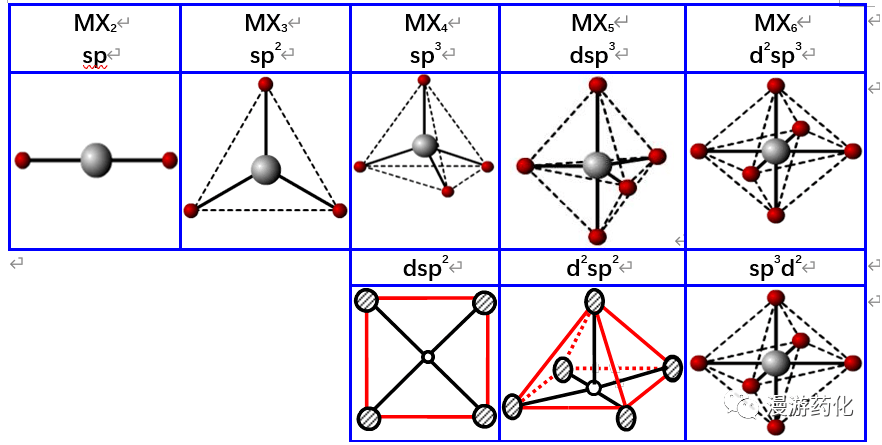
史上最易理解杂化轨道理论(图解)
立体几何 六面体切不出钝角直角三角形4

变形四面体形三角双锥形5角形三角锥形四面体形4角形平面三角形形3
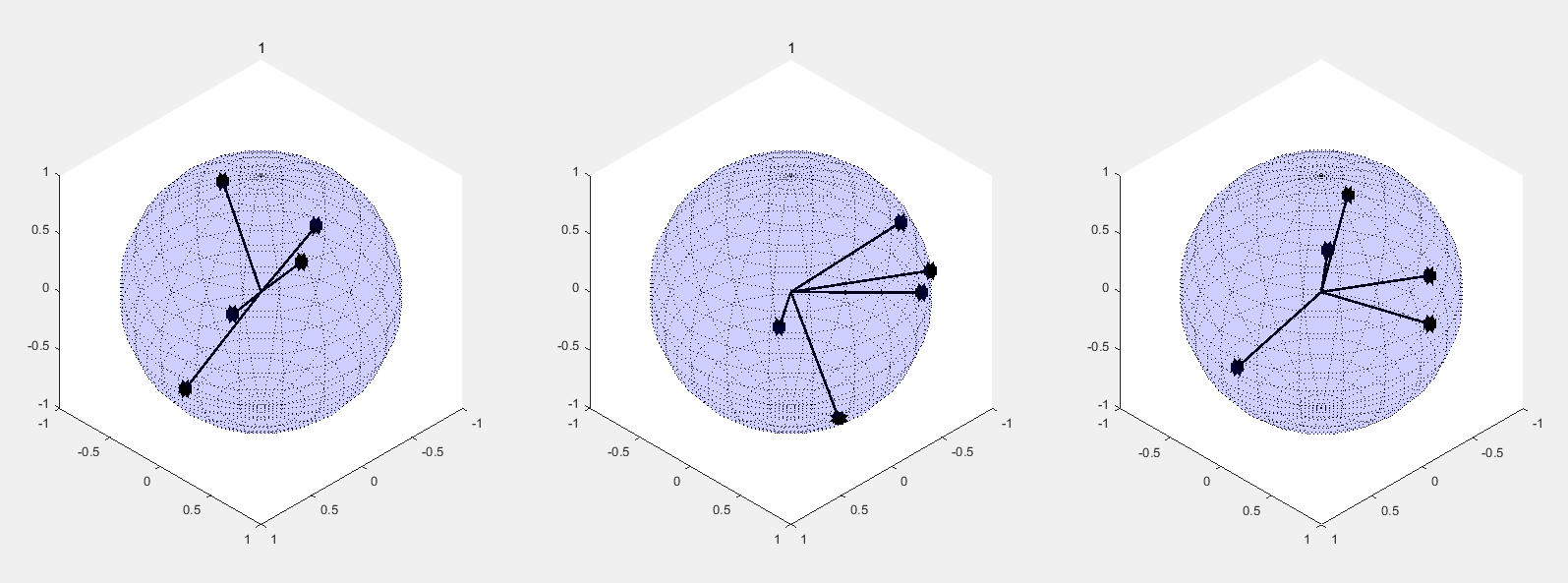
为什么 spd 杂化形成的是键角不等的三角双锥?
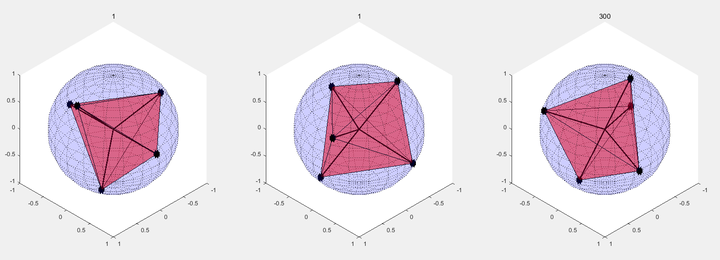
为什么sp06d杂化形成的是键角不等的三角双锥